В каких случаях доливать электролит в аккумулятор?
При проведении восстановительных мероприятий важно не нанести дополнительный вред аккумулятору. Ошибочная доливка электролита или воды может дополнительно нарушить электрохимический баланс и окончательно выведет из стоя элемент питания
Например, при сульфатации пластин происходит расход кислоты из раствора; для восполнения объема требуется заправка чистого электролита. При естественном испарении воды в банки необходимо заливать дистиллят, поскольку введение дополнительной серной кислоты вызовет ускоренную сульфатацию.
Необходимость пополнения запаса жидкости в аккумуляторе определяется по результатам замера уровня. Доливка чистого электролита возможна, если владелец точно знает объем утраченного вещества. В противном случае необходимо провести замер плотности раствора, что позволяет поддерживать оптимальную концентрацию серной кислоты.
Физические свойства сернокислотного электролита
Есть еще один физический фактор, который необходимо учитывать, особенно когда приготавливаются большие объемы раствора серной кислоты и дистиллированной воды. Это то обстоятельство, что при смешивании равных объемов серной кислоты и воды, после охлаждении такого раствора его объем будет меньше, чем сумма первоначальных объёмов. Что бы учесть этот фактор нужно обратится к четвертой таблице, в которой указаны величины уменьшения объёмов для растворов серной кислоты различной плотности.
Вязкость
Вязкость это свойство электролита, наиболее существенно влияющее на работоспособность свинцового аккумулятора. Электрохимические процессы, протекающие при работе аккумулятора, носят диффузионный характер. Скорость диффузии, в основном, зависит от вязкости электролита. Именно скоростью диффузии определяется поступление электролита к поверхности и в поры электродов при разряде, особенно при установке жестких (минутных, часовых) режимов разряда.
Чем вязкость выше, тем диффузия медленнее. При понижении температуры на 25С вязкость электролита возрастает в 2 раза, а при температуре в -50С она возрастает почти в 30 раз по сравнению с вязкостью при нормальной температуре. С увеличением вязкости падает ёмкость. Именно поэтому ра6отоспособность свинцовых аккумуляторов при низких температурах ухудшается. Это обстоятельство необходимо учитывать при установке герметичных аккумуляторов с гелевым (загущённым) электролитом.
Удельное сопротивление электролита
Сопротивление электролита, занимающего объем, ограниченный длиной 1 см и сечением в 1 см3, рассчитывается по формуле:
=rS/L
где r – удельное сопротивление Ом см;
L- длина, см.
S — поперечное сечение см2.
Сопротивление изменяется с изменением концентрации и температуры электролита.
Чтобы иметь минимальное внутреннее сопротивление АКБ, желательно применять электролит с наименьшим удельным сопротивлением.
Величины удельных сопротивлений приведены в таблице 5.
Таблица 5. Удельные сопротивления электролита
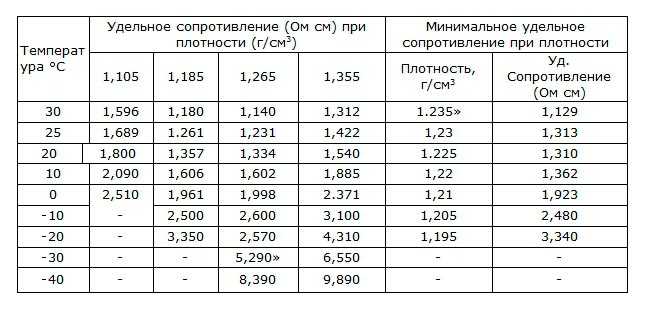
Удельное сопротивление электролита возрастает при снижении температуры, наиболее значительно при температуре 0С.
Температура замерзания электролита важна, постольку по мере разряда аккумулятора снижается его плотность и, соответственно, температура его замерзания. При замерзании объем электролита увеличивается, что приводит к разрушению сосуда и электродов аккумулятора. Наиболее низкую температуру замерзания имеет электролит плотностью 1,29 г/см3. Стартерные аккумуляторные батареи, эксплуатируемые в суровых условиях, имеют электролит плотностью 1,26-1,30 г/см3, который не замеряет при самых низких возможных температурах.
Для определения температур замерзания электролитов различной плотности следует пользоваться таблицей 6.
Как обслуживать свинцово-кислотный аккумулятор
По статистике 80% неполадок аккумулятора заключается в его сульфатации, появившейся из-за отсутствия технического обслуживания. Как проверить аккумулятор читайте здесь.
Чтобы предотвратить этот процесс, достаточно регулярно выполнять три процедуры:
- контролировать уровень дистиллированной воды;
- поддерживать чистоту;
- выравнивать заряд.
Как восстановить аккумулятор и убрать потерю емкости, читайте тут.
В процессе работы часть электролита испаряется, концентрация серной кислоты увеличивается, а уровень жидкости в банке понижается, что становится причиной контакта железных пластин с воздухом. Во избежание повреждения ячеек электродов нужно следить за количеством электролита и при необходимости добавлять в банку батареи дистиллированную воду.
Пользователи знают, насколько важна чистота АКБ: наличие грязи, пыли, подтёков кислоты может поспособствовать возникновению тока утечки, и аккумулятор разрядится и разбалансируется. Поэтому необходимо регулярно проводить чистку батареи, например, при помощи пароочистителя.
Чем чаще используется источник тока, тем больше ёмкость его ячеек будет отличаться друг от друга, что обязательно приведёт к проблемам в режиме зарядки. Чтобы урегулировать ситуацию, специалисты советуют пользоваться выравнивающим зарядным устройством, которое подаёт слабый ток и увеличивает время процесса на несколько часов, однако позволяет заряду распределиться равномерно и до 100% пополнить энергию.

Стандартное время зарядки пустой батареи составляет 10-12 часов
При этом крайне важно выставлять ток значением до 10% от ёмкости батареи. Обычно схема питания АКБ состоит из двух этапов: на первом аккумулятор заряжается постоянным током, на второй – постоянным напряжением
Чтобы осуществить проверку работоспособности, существует множество способов, как традиционных, так и современных. К последним относится контроль системы при помощи электронных тестеров, которые показывают более правильные результаты, но могут оказаться дорогостоящими. Конечно, без подобного оборудования не обойтись при проверке современных герметичных аккумуляторов. Но для более традиционных устройств подойдут простые методы, проверенные временем.
- Контроль плотности жидкости. При помощи ареометра нужно зарегистрировать значение плотности и сравнить с эталонными показателями. Для обеспечения нормальной работы параметр должен быть не ниже 1,23 г/см3, но не выше 1,4 г/см3.
- Контроль уровня электролита. Жидкость должна полностью покрывать свинцовые пластины и возвышаться на 1-1,5 см.
- Контроль с помощью нагрузочной вилки. Данное устройство измеряет напряжение АКБ под действием силы тока в десятки и сотни ампер. Такой метод весьма качественен для определения работоспособности батареи, однако, в случае частого использования нагрузочной вилки существует вероятность износа аккумулятора.
Порядок заливки и доливки кислотного электролита в АКБ
Составляющие компоненты электролита – кислоту и дистиллированную воду, нужно смешать в разных пропорциях. Так, если необходимо получить электролит с уровнем плотности 1,29 г/см³, то к 1 литру необходимо добавить 0,36 л кислоты, то есть в соотношении 1:3.
Заливку электролита производят стеклянной или полиэтиленовой трубочкой до уровня 10-15 мм над свинцовыми пластинами. После этого аккумулятор оставляют на два часа, однако в некоторых случаях плотность при этом падает. Далее АКБ заряжают током в десять раз меньшим его емкости в течение 4 часов.
Проверять плотность АКБ необходимо раз в 2-3 месяца. Для этого используется специальный прибор – ареометр.
Важно! В целях техники безопасности необходимо знать, что заливать нужно именно серную кислоту в дистилированную воду, но не наоборот, поскольку высока вероятность возникновения химической реакции данной смеси с выделением брызг и тепла
Применяемый вид кислоты
Одним из самых распространённых вопросов об АКБ является то, какую кислоту используют в аккумуляторе автомобиля.
Здесь есть разные теории и догадки. Одни считают, что в аккумуляторе автомобиля применяется сугубо соляная кислота. Другие, отвечая на вопрос о том, какая там кислота, говорят, что серная.
Нельзя сказать, что вопрос принципиальный для обычного автолюбителя, поскольку в чистом виде иметь дело с кислотой ему вряд ли придётся. Но при этом стоит знать, какая именно кислота находится в аккумуляторе. Это не соляная, а серная.
Если у вас вдруг спросят, какая кислота в действительности заливается в автомобильный аккумулятор, смело и уверенно отвечайте, что серная.
Существуют различные виды АКБ, где могут применяться иные жидкости в качестве электролита. В никель-кидмиевых устройствах это щёлочь. Есть и гелевые аппараты, где электролит имеет достаточно вязкую структуру, хотя по сути внутри находится та же кислота.
Если же говорить о том, какую кислоту на производстве заливают именно в свинцово-кислотный аккумулятор, используемый на автомобилях, то это будет серная.
В редких случаях с завода концентрация кислоты превышает 35%. Для решения задач, стоящих перед автомобильными АКБ, даже 30% вполне достаточно.
Зная теперь, какая именно кислота используется в автомобильных аккумуляторах, в какой концентрации и соотношении, можно переходить к ответам на другие вопросы.
Объективно недостаточно знать лишь то, какую кислоту при производстве батарей для автомобиля заливают в аккумулятор и какое альтернативное название она носит. Если вы планируете самостоятельно обслуживать и контролировать состояние АКБ, следует несколько расширить базу своих знаний. В последующем вам предстоит добавлять в АКБ электролит или просто подливать воду. Это вполне обычный процесс для обслуживаемых батарей.

Процессы, происходящие в АКБ с участием электролита
Работа свинцово-кислотного автомобильного аккумулятора основывается на электрохимических процессах, которые протекают с участием электролита. Аккумулятор автомобиля состоит из положительных и отрицательных пластин, погруженных в водный раствор серной кислоты. Положительные и отрицательные пластины имеют токоотводящие решётки из свинца с различными добавками в зависимости от типа аккумулятора.
На решётках положительных электродов нанесён красновато-коричневый диоксид свинца (PbO2). На отрицательных электродах — сероватый порошок свинца (Pb). Электрические характеристики аккумулятора напрямую зависят от плотности электролита. Для понимания назначения электролита нужно рассмотреть основные процессы, происходящие в аккумуляторе автомобиля.
При разряде аккумулятор на положительном электроде (аноде) идёт следующая реакция:
PbO2 + SO42− + 4H+ + 2e− -> PbSO4 + 2H2O
На отрицательном электроде (катоде) протекает такой процесс:
Pb + SO42− − 2e− ->PbSO4
При заряде АКБ эти реакции протекают в обратном направлении.
3324
В начале разрядки процесс диффузии кислоты в электроды. Это объясняется тем, что в активной массе электродов поры ещё не забиты сульфатом. По мере того, как на них образуется слой сульфата и забивает поры, процесс диффузии притормаживается. В теории процесс разряда может идти до того момента, пока электролит не превратится в воду. Но на практике разряд идёт до тех пор, пока плотность не опуститься до значения 1,15 гр/см3. К моменту падения плотности до 1,15 гр/см3 выделяется столько сульфата свинца, что его хватило для закупоривания активной массы пластин. По плотности электролита можно судить о степени заряженности АКБ. Для этого можно использовать таблицу, представленную ниже.
| Плотность электролита, г/см. куб. (+15 гр. Цельсия) | Напряжение, В (в отсутствии нагрузки) | Напряжение, В (с нагрузкой 100 А) | Степень заряда АКБ, % | Температура замерзания электролита, гр. Цельсия |
|---|---|---|---|---|
| Плотность электролита, г/см. куб. (+15 гр. Цельсия) | Напряжение, В (в отсутствии нагрузки) | Напряжение, В (с нагрузкой 100 А) | Степень заряда АКБ, % | Температура замерзания электролита, гр. Цельсия |
| 1,11 | 11,7 | 8,4 | -7 | |
| 1,12 | 11,76 | 8,54 | 6 | -8 |
| 1,13 | 11,82 | 8,68 | 12,56 | -9 |
| 1,14 | 11,88 | 8,84 | 19 | -11 |
| 1,15 | 11,94 | 9 | 25 | -13 |
| 1,16 | 12 | 9,14 | 31 | -14 |
| 1,17 | 12,06 | 9,3 | 37,5 | -16 |
| 1,18 | 12,12 | 9,46 | 44 | -18 |
| 1,19 | 12,18 | 9,6 | 50 | -24 |
| 1,2 | 12,24 | 9,74 | 56 | -27 |
| 1,21 | 12,3 | 9,9 | 62,5 | -32 |
| 1,22 | 12,36 | 10,06 | 69 | -37 |
| 1,23 | 12,42 | 10,2 | 75 | -42 |
| 1,24 | 12,48 | 10,34 | 81 | -46 |
| 1,25 | 12,54 | 10,5 | 87,5 | -50 |
| 1,26 | 12,6 | 10,66 | 94 | -55 |
| 1,27 | 12,66 | 10,8 | 100 | -60 |
Если разряжать аккумулятор автомобиля небольшим током (10 процентов от номинальной ёмкости), то через час разрядки напряжение элемента снижается до 2 вольт. Это происходит из-за того, что в этом момент быстро формируется большое количество PbSO4, который забивает поры активной массы. В результате растёт внутреннее сопротивление элементов АКБ и падает концентрация электролита. Через некоторое время процесс разрядки выходит на прямую (см. график).
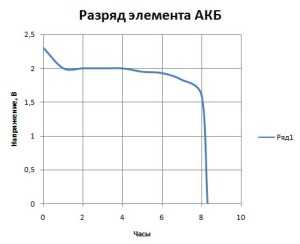
График разрядки аккумулятора
Типы и характеристики электролитов
Электролит изготавливается смешиванием концентрированной серной кислоты и дистиллированной воды в строго определенных пропорциях. Для изготовления электролита используется специальная аккумуляторная серная кислота (по ГОСТ 667-73) и дистиллированная вода (по ГОСТ 6709-72). Данный раствор используется во всех типах современных свинцово-кислотных аккумуляторов.
Главная характеристика электролита — плотность. Для нормальной работы АКБ плотность электролита должна лежать в пределах 1,23-1,4 г/куб. см, так как именно при такой плотности раствор имеет максимальную электропроводность. Однако плотность концентрированной серной кислоты составляет 1,83 г/куб. см, поэтому для достижения необходимой плотности кислота смешивается с водой.
Плотность электролита в значительной степени зависит от двух параметров: температуры и степени заряда аккумулятора.
О зависимости плотности электролита в зависимости от заряда АКБ мы сказали выше: при заряде плотность повышается, при разряде — понижается. Зависимость плотности электролита от температуры простая: при снижении температуры плотность падает, при повышении — возрастает. Поэтому нормальная плотность определяет при температуре +25°C, а чтобы верно измерять плотность при любой температуре, используют таблицу поправок к показаниям ареометра:
| Температура электролита,°C | Поправка к показаниям ареометра,г/куб. см |
|---|---|
| -55 … -41 | -0,05 |
| -40 … -26 | -0,04 |
| -25 … -11 | -0,03 |
| -10 … +4 | -0,02 |
| +5 … +19 | -0,01 |
| +20 … +30 | |
| +31 … +45 | +0,01 |
| +46 … +60 | +0,02 |
Например, если электролит при температуре +25°C имеет плотность 1,28 г/куб. см, то при температуре -15°C он имеет плотность 1,25 г/куб. см, а при нагреве до +50°C (что часто бывает в подкапотном пространстве автомобиля) плотность повышается до 1,3 г/куб. см.
Чтобы компенсировать изменение плотности электролита в АКБ транспортных средств, эксплуатируемых в различных климатических поясах, применяются электролиты большей или меньшей плотности:
- Летние и для жаркого климата — плотностью 1,23-1,24 г/куб.см;
- Для умеренного и холодного климата — 1,27-1,28 г/куб.см;
- Зимние и для холодного климата — 1,3-1,34 г/куб.см.
Кроме того, при повышении плотности электролита повышается его морозоустойчивость — более плотные электролиты устойчивы к замерзанию, поэтому они лучше подходят для эксплуатации в холодное время года и в холодных климатических поясах.
Сегодня можно купить электролит необходимой плотности, освободив себя от непростой процедуры приготовления правильного по характеристикам электролита из кислоты и воды. Электролит продается в тарах емкостью от 1 до 20 литров, поэтому всегда можно приобрести нужный для работы объем.
Для чего нужна кислота
Прежде чем приступать к описанию процессов, протекающих при разряде/заряде, стоит сразу сказать, какая кислота используется в аккумуляторе любого автомобиля – это серная (H2SO4), а не соляная или, например, фосфорная.
Она необходима для приготовления электролита – жидкости, в которой присутствуют заряженные частицы – ионы. Электролит представляет собой не просто пассивный раствор, в котором частицы воды и кислоты перемешаны друг с другом. Это активная жидкость, отличительная особенность которой – постоянное протекание в ней взаимно исключающих друг друга процессов – диссоциации и ассоциации.
 В аккумуляторе присутствует серная кислота
В аккумуляторе присутствует серная кислота
При диссоциации, которая протекает лишь в водном растворе H2SO4. Молекулы кислоты образуют ионы с положительными и отрицательными зарядами:
 Диссоциация кислоты
Диссоциация кислоты
Параллельно с диссоциацией протекает обратный процесс – превращение ионов в молекулы кислоты. Полной ионизации электролита, а также полной нейтрализации заряженных частиц не происходит. Процессы находятся в динамическом равновесии, которое может измениться лишь под влиянием внешнего воздействия.
Именно наличие ионов и превращает раствор в электролит. Под влиянием электрического поля (во время зарядки) заряженные частицы переносят заряд к пластинам аккумулятора. При реакции между ионами и веществом пластин происходит высвобождение электронов. Они способны двигаться по проводнику при подключении его к электродам (их выводам).
Основные процессы, протекающие при разряде
Отрицательные пластины АКБ и их обмазка изготовлены из свинца (Pb), а у положительных активная масса имеет основой его диоксид (PbO2). Металлический свинец обладает большим количеством свободных электронов, чем его диоксид. Если положительную и отрицательную пластины соединить проводником, то разность потенциалов практически сразу уравновесится и электрический ток не возникнет.
Но если эти пластины погрузить в сернокислотный электролит, то перенос электронов вызовет химические реакции окисления металлического свинца и восстановления его диоксида:
PbO2 + SO42- + 4H++ 2e- = PbSO4 + H2O
Как видите, «конечными продуктами» этих реакций являются:
- Сульфат свинца PbSO4, образующийся на поверхности пластин.
- Вода.
- Свободные электроны (e-), благодаря которым и возникает электрический ток.
При достаточно продолжительном разряде серная кислота может полностью «израсходоваться» на образование сульфата и воды, в результате чего прекратятся химические реакции и свободные электроны не будут образовываться. Поэтому особенно ценным в плане практического использования свинцовых аккумуляторных батарей является возможность протекания обратных реакций при подключении к выводам электрического напряжения.
При зарядке сульфат свинца, прореагировав с водородом, снова становится серной кислотой, в результате чего плотность электролита восстанавливается, а поверхность пластин аккумулятора приобретает первоначальный состав.
 Проверка плотности электролита
Проверка плотности электролита
Что потребуется для замены электролита в аккумуляторах?
Набор приборов и инструментов зависит от того, какой метод залива и слива вы будете использовать. Сразу заметим, что полностью менять электролит не имеет смысла. Если его состав уже сильно изменился, это говорит о приближающейся смерти батареи. Намного проще сразу купить новый аккумулятор и не переживать о том, что он может выйти из строя в любой момент.
Также выбор комплекта инструментов зависит от того, как электролит заливать в аккумулятор. Часто можно использовать готовые жидкости, которые продаются в автомобильных магазинах. Но готовый электролит может не подойти для вашего аккумулятора. Поэтому в большинстве случаев разбавляют жидкость в банках батареи дистиллированной водой. Правда, эта мера временная и не приносит устойчивого результата.
Применение серной кислоты и её сорта
Вообще, в качестве электролита в некоторых видах автомобильных аккумуляторов может использоваться щёлочь. Например, никель-кадмиевый или никель-железный тип АКБ. Есть ещё группа гелевых аккумуляторов AGM и GEL, где электролит находится в связанном состоянии. Но это тот же раствор серной кислоты. Просто он либо переведён в гелеобразное состояние с помощью добавок (GEL), либо им пропитано стекловолокно (AGM). Наиболее распространёнными на сегодняшний день остаются свинцово-кислотные автомобильные аккумуляторы с жидким электролитом. Поэтому речь пойдёт именно о водном растворе серной кислоты, предназначенном для заливки в АКБ.
Электролит
Дистиллированная вода
Серная кислота используется в самых разных отраслях народного хозяйства. К примеру, с её помощью очищается поверхность металла перед нанесением покрытия, она используется при приготовлении различных синтетических красителей. Кроме того, серная кислота востребована в сфере производства удобрений, взрывчатки, фармакологической промышленности, переработке нефти.
243
Существуют основные сорта серной кислоты, которые перечислены ниже:
- Башенная или нитрозная. Концентрация 75 процентов. Плотность этого сорта составляет 1,67 гр/см3. Название этот сорт получил из-за метода производства в футерованных башнях нитрозным способом. Обжиговый газ с двуокисью серы (SO2) обрабатывается нитрозой (H2SO4 с добавками оксидов азота). В ходе химической реакции получается оксиды азота и кислота. При этом оксиды постоянно циркулируют в производственном цикле;
- Контактная. Концентрация от 92,5 до 98 процентов. Плотность сорта составляет 1,837 гр/см3. Этот сорт также производится из обжигового газа, в котором содержится двуокись SO2. В ходе реакции происходит ее окисление до SO3 при контакте с твёрдым катализатором из ванадия;
- Сорт Олеум. Концентрация 104,5 процента. Плотность составляет 1,897 гр/см3. Сорт представляет собой раствор SO3 в серной кислоте (H2SO4). Соотношение SO3 — 20 процентов, H2SO4 — 104,5 процента;
- Высокопроцентный олеум. Концентрация 114,6 процента, а плотность 2,002 гр/см3;
- Аккумуляторная. Концентрация от 92 до 94 процента, а плотность 1,835 гр/см3.
Классификация
Исходя из степени диссоциации все электролиты делятся на две группы:
- Сильные электролиты — электролиты, степень диссоциации которых в растворах равна единице (то есть диссоциируют полностью) и не зависит от концентрации раствора. Сюда относятся подавляющее большинство солей, щелочей, а также некоторые кислоты (сильные кислоты, такие как HCl, HBr, HI, HNO3, H2SO4).
- Слабые электролиты — степень диссоциации меньше единицы (то есть диссоциируют не полностью) и уменьшается с ростом концентрации. К ним относят воду, ряд кислот (слабые кислоты, такие как HF), основания p-, d- и f-элементов.
Между этими двумя группами чёткой границы нет, одно и то же вещество может в одном растворителе проявлять свойства сильного электролита, а в другом — слабого.
Сколько должно быть электролита в аккумуляторах разного объёма
Как известно, в зависимости от объёма двигателя подбирается источник питания. Будет ли одинаков объём электролита в аккумуляторе ёмкостью 60 А/ч и 35 А/ч? Конечно же, нет. Чем мощнее устройство, тем больше его габариты, а следовательно, большее внутреннее пространство корпуса АКБ нужно заполнить. Рассмотрим подробнее, сколько электролита и в каком аккумуляторе должно быть.
В самом популярном для легковых авто аккумуляторе ёмкостью 55 А/ч объём электролита составляет примерно 2,5 литра, что в общем-то совсем немного.
А вот на автобусах применяют батареи, ёмкостные характеристики которых в разы превосходят аналогичный параметр стандартных машин. Тогда сколько электролита требуется залить в аккумулятор, если его ёмкость равна 190 А/ч? Ориентировочно во столько же раз больше, во сколько раз отличаются их величины мощности.
На современных внедорожниках установлены источники энергии увеличенной мощности, ведь и двигатель у них большего объёма. Сколько вмещается электролита в аккумулятор ёмкостью 75 А/ч? Опять же, если взять за базовую величину самый востребованный, то, вычислив разницу в их ёмкости, несложно определить и нужный объём жидкости.
АКБ на 60 А/ч чаще встречаются в автомобилях иностранного производства. Сколько литров электролита должно быть в аккумуляторе ёмкостью 60 А/ч? Этот объём тоже невелик и в зависимости от его производителя находится в пределах от 2,7 до 3 литров.
Как-то привычно, что весь модельный ряд источников энергии кратен цифре пять. Но оказывается, есть модель, которая выбивается из установленной закономерности. Сколько нужно электролита, чтобы заполнить свободное пространство в аккумуляторе ёмкостью 62 А/ч, который используют на автомобилях ГАЗ? Это количество практически не отличается от 60-амперного устройства.
Теперь становится ясно, сколько электролита заливать в каждый аккумулятор – всё зависит от его параметров и габаритов.













